Le système urinaire (cours 3)
Dans cette leçonci nous décrirons les autres
segments du néphron, tous tubulaires. Chacun d'eux possède
des caractères histologiques étroitement liés
à sa physiologie. C'est pourquoi, en analysant leur structure,
nous évoquerons systématiquement leur fonction.
 Reprenons le schéma général du néphron:
au glomérule fait suite la partie contournée
du tube proximal puis sa partie droite (en vert), le segment
grêle (en gris), la partie droite du tube distal
et sa partie contournée (en brun), s'abouchant à
un tube collecteur (en jaune) qui draine l'urine de plusieurs
néphrons vers l'orifice papillaire. Rappelons que la partie
droite du tube proximal, le segment grêle et la partie droite
du tube distal forment ensemble l'anse de Henlé.
Reprenons le schéma général du néphron:
au glomérule fait suite la partie contournée
du tube proximal puis sa partie droite (en vert), le segment
grêle (en gris), la partie droite du tube distal
et sa partie contournée (en brun), s'abouchant à
un tube collecteur (en jaune) qui draine l'urine de plusieurs
néphrons vers l'orifice papillaire. Rappelons que la partie
droite du tube proximal, le segment grêle et la partie droite
du tube distal forment ensemble l'anse de Henlé.
Dans une coupe de rein
examinée à faible grossissement, les différents
segments tubulaires peuvent déjà être distingués
les uns des autres parce qu'ils ont une coloration, une taille,
une localisation et une morphologie différentes. Ainsi,
dans le cortex, les tubes très colorés et relativement
larges sont des tubes proximaux. Dans la médullaire, les
tubes les plus larges sont des tubes collecteurs.
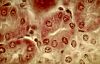 Le calibre du tube proximal,
d'environ 60 micromètres, est plus important que celui
des autres segments tubulaires corticaux. Les cellules sont pyramidales.
Leur pôle apical est muni d'une bordure en brosse
qui comble partiellement la lumière. Le cytoplasme est
éosinophile parce qu'il est particulièrement
riche en mitochondries et relativement pauvre en ribosomes.
Le noyau rond est central.
Le calibre du tube proximal,
d'environ 60 micromètres, est plus important que celui
des autres segments tubulaires corticaux. Les cellules sont pyramidales.
Leur pôle apical est muni d'une bordure en brosse
qui comble partiellement la lumière. Le cytoplasme est
éosinophile parce qu'il est particulièrement
riche en mitochondries et relativement pauvre en ribosomes.
Le noyau rond est central.
La bordure en brosse
du pôle apical est composée de microvillosités;
entre elles s'ouvrent des invaginations qui s'enfoncent dans le
cytoplasme et sont entourées de vésicules et de
vacuoles. L'ensemble représente une très grande
surface membranaire en rapport avec la fonction d'absorption.
La bordure en brosse se trouve aussi bien dans la partie contournée
que dans la partie droite du tube proximal. Elle n'existe pas
dans les segments suivants. Comme dans d'autres épithéliums
de revêtement, les membranes latérales, non visibles
dans cette micrographie, sont interdigitées les unes dans
les autres et possèdent près de la lumière
tubulaire des systèmes de jonctions serrées
qui empêchent le passage de l'eau et des solutés.
Le pôle basal
est strié par de profondes invaginations membranaires,
perpendiculaires à la membrane basale, visible sous la
forme d'un liseré gris. Dans le cytoplasme de ce pôle,
les mitochondries sont longues et nombreuses. Elles forment
des files plus ou moins parallèles, enchâssées
entre les invaginations de la membrane plasmique. L'importance
des mitochondries démontre que les cellules des tubes proximaux
produisent et consomment de grandes quantités d'énergie.
Le tube proximal est essentiel car c'est lui qui assure la partie
la plus importante de la réabsorption tubulaire.
Il est aussi sécréteur.
La réabsorption du sodium y est prépondérante:
70% du sodium de l'urine primitive sont récupérés
au niveau du tube proximal. L'eau suit en quantité proportionnelle
et la concentration en sodium dans la lumière du tube est
donc constante. Le sodium diffuse passivement à travers
la membrane apicale, en fonction de la différence de sa
concentration dans le tube et dans la cellule. Cette différence
est maintenue grâce à une extraction active du
sodium de la cellule par des pompes ATPasedépendantes,
situées dans les membranes basolatérales.
Ce transport actif qui n'est jamais saturé consomme 80%
de l'énergie produite dans le rein. A partir de l'interstitium,
le sodium et l'eau diffusent dans les capillaires.
Les autres cations, tels le potassium, le calcium et le magnésium,
sont aussi réabsorbés en majeure partie au niveau
proximal; comme celle du sodium, leur réabsorption est
isoosmotique, c'est à dire qu'elle s'accompagne
d'une quantité d'eau équivalente.
Normalement les acides aminés et le glucose sont
totalement réabsorbés. Cependant, si leur concentration
sanguine dépasse un certain seuil, ils sont éliminés
dans l'urine en quantités proportionnelles à la
surcharge sanguine.
L'urée, l'acide urique et les acides organiques,
comme les acides acétoglutarique,
acétoacétique et bhydroxybutyrique
sont, eux aussi, totalement récupérés si
leur concentration dans l'urine primitive ne dépasse pas
un certain seuil.
Les petites protéines qui parviennent à franchir
le filtre glomérulaire, telles l'insuline et de très
petites quantités d'albumine, sont endocytées
puis hydrolysées par le système lysosomial
des cellules du tube proximal. Le rein est ainsi un lieu important
de dégradation des protéines plasmatiques dont le
poids moléculaire ne dépasse pas 70.000.
Les phosphates et le bicarbonate sont également
réabsorbés au niveau du tube proximal. La balance
entre leur réabsorption et leur élimination possible
en cas d'excès intervient dans le maintien de l'équilibre
acidebase.
Les bicarbonates
sont d'abord transformés en CO2 et en eau par l'anhydrase
carbonique des microvillosités. L'eau et le CO2 diffusent
dans la cellule et reforment du bicarbonate sous l'effet d'une
anhydrase carbonique cytoplasmique. Ce bicarbonate est dissocié;
l'ion HCO3 diffuse dans le sang; l'ion H+ diffuse dans la
lumière du tube.
Le tube proximal est aussi sécréteur. Comme
nous venons de le voir, il élimine des protons qui
se lient aux ions bicarbonates. Il sécrète de faibles
quantités d'urée, seul produit à y être
à la fois excrété et réabsorbé.
Enfin, il élimine sélectivement des produits exogènes,
tels que certains médicaments.
Le deuxième segment des tubes rénaux est le segment
grêle qui constitue la partie descendante de l'anse
de Henlé et, dans les néphrons les plus longs, une
portion de sa branche ascendante près du sommet de l'anse.
Dans une coupe histologique,
obtenue après enrobage à la paraffine et colorée
selon les méthodes habituelles, l'identification des segments
grêles est aisée lorsqu'il est possible, comme ici,
d'observer leur origine à partir du tube proximal. La transition
épithéliale est brusque; l'épithélium
à bordure en brosse de l'un se transforme en épithélium
très aplati de l'autre.
Lorsque cette transition ne s'observe pas, le segment grêle
est plus difficile à reconnaître. Son calibre est
très étroit et sa lumière est ténue.
Son épithélium, désigné ici par une
flèche, est aplati, mais le cytoplasme reste visible
et les noyaux ne font pas saillie dans la lumière,
contrairement à ce que l'on observe dans l'endothélium
du capillaire, désigné par une tête de flèche.
Il n'y a pas de différence morphologique entre la partie
descendante et la partie ascendante du segment grêle. Toutes
deux sont situées dans la médullaire.
Le segment grêle du néphron est très perméable
à l'eau et aux électrolytes mais pas du tout à
l'urée. La diffusion passive de l'eau et du sodium à
travers ce segment intervient dans l'établissement du gradient
d'osmolarité corticopapillaire suivant un mécanisme
qui sera expliqué plus loin.
Le troisième segment tubulaire est le tube distal.
Il comprend trois parties: la partie droite qui entre dans
la constitution de la branche ascendante de l'anse de Henlé
et est située d'abord dans la médullaire puis dans
le cortex, la partie contournée située dans
le cortex et la macula densa qui est à la jonction
des deux précédentes.
Dans cette coupe histologique
colorée selon une technique trichromique classique, les
tubes distaux ont à peu près le même diamètre
que les tubes proximaux. Ils sont plus clairs et leur paroi
est composée de cellules cubiques dont le pôle
apical est dépourvu de bordure en brosse. Comparée
à celle des tubes proximaux, leur lumière est plus
large.
Le pôle apical
des cellules du tube distal est dépourvu de microvillosités.
Il existe cependant de courtes expansions cytoplasmiques
dont le nombre est variable et qui donnent à ce pôle
un aspect irrégulier. Le pôle basal ressemble à
celui des cellules du tube proximal. Il est strié perpendiculairement
par de longues mitochondries enserrées entre des
invaginations de la membrane plasmique. Ici encore l'importance
des mitochondries démontre que les cellules du tube distal
produisent et consomment de grandes quantités d'énergie.
La partie droite du tube distal a une propriété
essentielle : elle extrait de façon active le sodium
de la lumière tubulaire vers l'interstitium adjacent. Sa
paroi est par contre imperméable à l'eau comme
à l'urée. Le transport actif du sodium provoque
donc une augmentation de l'osmolarité de l'interstitium
qui n'est pas compensée à ce niveau par un flux
d'eau. Ce transport actif est le moteur qui établit le
gradient d'osmolarité corticopapillaire, comme nous
le verrons ultérieurement.
Le rôle principal de la portion contournée
du tube distal est la production d'ammoniaque et de protons.
Elle réabsorbe en faible quantité du sodium, du
calcium et des phosphates. Elle élimine du potassium; cette
élimination est passive, consécutive et proportionnelle
à l'électronégativité du contenu tubulaire,
qui dépend de sa concentration en ions Cl. L'excrétion
urinaire de potassium est donc directement proportionnelle à
la réabsorption distale de sodium.
La macula densa
est la portion épithéliale du tube distal, appliquée
contre le glomérule rénal entre les artérioles
afférente et efférente. Elle est composée
de cellules plus hautes et plus étroites que les
autres cellules du tube. Leurs noyaux sont tous situés
à la même hauteur. La macula densa est séparée
des cellules du coussinet polaire par une membrane basale très
mince et discontinue. La macula densa et le coussinet polaire
appartiennent à l'appareil juxtaglomérulaire.
Les chémorécepteurs de la macula densa réagissent
à l'hypertonicité osmotique de l'urine et
les barorécepteurs de l'artériole afférente
réagissent à l'hypotension sanguine. A la suite
de cette stimulation, le coussinet polaire sécrète
une enzyme, la rénine, qui scinde l'angiotensinogène,
protéine plasmatique, en angiotensine 1 qui à son
tour est modifiée par une enzyme plasmatique en angiotensine
2. Celleci a une action vasoconstrictrice extrêmement
puissante et stimule la sécrétion d'aldostérone
corticosurrénalienne, activant ainsi la réabsorption
sodée dans le tube distal. Elle stimule aussi le centre
hypothalamique de la soif. Par ses différents effets elle
accroît la récupération d'eau et augmente
ainsi la volémie.
 Le tube collecteur
dérive du bourgeon urétéral tandis que les
néphrons proviennent du métanéphros. Il draine
plusieurs néphrons vers l'extrémité papillaire
où il est appelé tube de Bellini. Près
de son origine, la paroi du tube collecteur est constituée
de cellules cubiques claires qui délimitent une
lumière assez importante.
Le tube collecteur
dérive du bourgeon urétéral tandis que les
néphrons proviennent du métanéphros. Il draine
plusieurs néphrons vers l'extrémité papillaire
où il est appelé tube de Bellini. Près
de son origine, la paroi du tube collecteur est constituée
de cellules cubiques claires qui délimitent une
lumière assez importante.
Plus on se rapproche de la médullaire,
plus ces cellules deviennent cylindriques et de taille irrégulière.
Elles ne sont pas striées et sont dépourvues de
microvillosités.
 Le tube collecteur
joue un rôle important dans l'économie d'eau
et dans la concentration finale de l'urine, éventuellement
audelà de l'osmolarité plasmatique qui est
d'environ 300 mosm. Il doit cette fonction à son trajet
particulier qui lui fait traverser un milieu hypertonique.
Né dans le cortex profond de la confluence de plusieurs
tubes contournés distaux, il rejoint le sommet d'une papille
en traversant la médullaire ou règne une pression
osmotique supérieure à celle du plasma et de plus
en plus élevée au fur et à mesure que l'on
se rapproche du sommet de la papille. En l'absence d'hormone
antidiurétique, situation figurée dans la partie
gauche du schéma, le tube collecteur est imperméable
à l'eau. L'urine, devenue hypotonique depuis la traversée
de l'anse de Henlé, le parcourt pratiquement sans modification
jusqu'à son excrétion dans le calice. L'émission
d'une urine hypotonique a lieu chaque fois que l'organisme dispose
d'eau en excès. En cas de pénurie d'eau, il y a
sécrétion d'hormone antidiurétique
par la neurohypophyse qui réagit à la diminution
globale du volume sanguin et à l'augmentation de la pression
osmotique du milieu intérieur. L'hormone antidiurétique
rend la paroi du tube collecteur perméable à
l'eau, situation décrite dans la moitié droite du
schéma. A cause de la grande différence de pression
osmotique de part et d'autre de la paroi tubulaire, l'eau diffuse
du tube vers le milieu interstitiel de la médullaire et
l'urine se concentre.
Le tube collecteur
joue un rôle important dans l'économie d'eau
et dans la concentration finale de l'urine, éventuellement
audelà de l'osmolarité plasmatique qui est
d'environ 300 mosm. Il doit cette fonction à son trajet
particulier qui lui fait traverser un milieu hypertonique.
Né dans le cortex profond de la confluence de plusieurs
tubes contournés distaux, il rejoint le sommet d'une papille
en traversant la médullaire ou règne une pression
osmotique supérieure à celle du plasma et de plus
en plus élevée au fur et à mesure que l'on
se rapproche du sommet de la papille. En l'absence d'hormone
antidiurétique, situation figurée dans la partie
gauche du schéma, le tube collecteur est imperméable
à l'eau. L'urine, devenue hypotonique depuis la traversée
de l'anse de Henlé, le parcourt pratiquement sans modification
jusqu'à son excrétion dans le calice. L'émission
d'une urine hypotonique a lieu chaque fois que l'organisme dispose
d'eau en excès. En cas de pénurie d'eau, il y a
sécrétion d'hormone antidiurétique
par la neurohypophyse qui réagit à la diminution
globale du volume sanguin et à l'augmentation de la pression
osmotique du milieu intérieur. L'hormone antidiurétique
rend la paroi du tube collecteur perméable à
l'eau, situation décrite dans la moitié droite du
schéma. A cause de la grande différence de pression
osmotique de part et d'autre de la paroi tubulaire, l'eau diffuse
du tube vers le milieu interstitiel de la médullaire et
l'urine se concentre.
Quel est le mécanisme qui crée et entretient le
gradient osmotique dans la médullaire rénale? Il
s'agit d'un système de concentration par contrecourant.
Un tel système comprend un tube coudé en épingle
à cheveu dans lequel circule une solution et au niveau
duquel il existe un transfert actif de soluté de
la branche ascendante vers la branche descendante. De cette façon,
un effet de concentration relativement faible mais répété
tout au long du tube permet la création d'un milieu
très concentré au sommet de l'anse. Dans la
médullaire rénale un tel système est constitué
par l'anse de Henlé qui fonctionne de la manière
suivante.
Supposons d'abord que la pression osmotique soit de 30 mosm dans
tout le système et que le liquide soit immobile. Cette
situation de départ théorique est représentée
dans la figure 1. La branche descendante de l'anse est librement
perméable à l'eau et aux électrolytes, si
bien que son contenu sera constamment en équilibre osmotique
avec le milieu péritubulaire. La paroi de la branche ascendante
est imperméable à l'eau mais elle possède
des pompes à sodium représentées par des
cercles.
Lorsque ces pompes démarrent (figure 2), elles créent
un gradient osmotique de 200 mosm entre le contenu de la branche
ascendante et le milieu péritubulaire. Comme la branche
descendante est librement perméable, la pression osmotique
de son contenu et celle du milieu péritubulaire s'équilibrent
immédiatement.
Si maintenant le liquide se déplace de la branche descendante
vers la branche ascendante, les pompes étant supposées
à l'arrêt (figure 3), la différence d'osmolarité
entre la branche ascendante et le milieu péritubulaire
diminue au sommet de l'anse, car de l'urine concentrée
à 400 mosm entre dans la branche ascendante.
Dès qu'elles démarrent (figure 4), les pompes à
sodium rétablissent le gradient de 200 mosm entre le contenu
de la branche ascendante et le milieu péritubulaire, toujours
en équilibre avec la branche descendante. L'effet global
est une augmentation de la pression osmotique au sommet de la
boucle. En même temps l'urine qui quitte la branche ascendante
est devenue hypotonique.
Ce cycle se répète et crée un gradient osmotique
de plus en plus élevé (figure 5). Dans la réalité,
l'activité des pompes et le déplacement du liquide
sont évidemment simultanés et continus. Le gradient
final obtenu avec des pompes d'une "puissance" de 200
mosm et pour un flux de liquide constant dépend de la longueur
de l'anse. Chez l'homme, la pression osmotique au sommet de la
papille est voisine de 1.200 mosm, soit quatre fois la
valeur plasmatique.
Pour que le système soit efficace, il faut éviter
l'élimination trop rapide des solutés au niveau
de la papille. Ceci se produirait immanquablement si les vaisseaux
irriguant la papille la traversaient seulement dans un sens. En
effet, comme les échanges d'eau et d'électrolytes
se font librement à travers la paroi vasculaire, les ions
diffuseraient du milieu hyperconcentré de la papille vers
le plasma sanguin, tandis que de l'eau sortirait du lit vasculaire
et diluerait le liquide interstitiel. C'est pourquoi les vaisseaux
de la médullaire rénale, les "vasa recta",
ont la même disposition que les anses de Henlé.
Au niveau de la branche vasculaire descendante, le sang se
concentre au fur et à mesure qu'il s'écoule
vers le sommet de la papille à cause de la sortie d'eau
et de l'entrée des ions. Dans la branche ascendante,
les mouvements inverses ont lieu et le sang quittant la médullaire
n'est que légèrement hypertonique. Les anses
vasculaires forment donc un système d'échange passif
par contrecourant qui minimise la perte des solutés
au niveau de l'espace interstitiel de la papille. Le léger
excès de pression osmotique du sang qui quitte la médullaire
permet le pompage de l'eau qui est récupérée
par le tube collecteur lorsque celuici est sous l'influence
de l'hormone antidiurétique.
Rappelons que les "vasa recta" sont des capillaires
issus des artérioles efférentes. Ils plongent dans
la médullaire où ils se groupent en faisceaux autour
des branches des anses de Henlé. Ces longs faisceaux se
repèrent aisément dans une coupe histologique
observée à faible grossissement. Cette image montre
le trajet apparemment rectiligne auquel ces vaisseaux doivent
leur nom. Nous venons de voir qu'en réalité il s'agit
de boucles vasculaires très allongées.
Nous avons ainsi terminé la description des différents
segments du néphron et de leur fonction individuelle. En
résumant brièvement ces différentes fonctions,
nous pourrons expliquer comment, à partir du plasma, on
peut obtenir l'urine définitive.
Le glomérule rénal filtre le plasma. L'ensemble
des glomérules rénaux produisent 125 ml d'urine
primitive par minute, soit, dans les conditions normales,
180 litres par jour. Cette urine primitive est collectée
dans les espaces urinaires de Bowman. La plus grande partie, environ
70%, est réabsorbée dans le cortex au niveau
du tube proximal qui assure aussi la récupération
du glucose, des acides aminés et d'autres substances ne
devant pas être éliminées.
A la sortie du tube proximal le volume urinaire est encore de
54 litres par jour, dont la majeure partie est réabsorbée
au niveau du tube distal, si bien qu'à la sortie
de ce tube le volume urinaire ne représente plus que 10%
du volume de l'urine primitive, soit environ 18 litres. Ceuxci
seront réduits à environ 1,5 litre dans le tube
collecteur dans la mesure où celuici est influencé
par l'hormone antidiurétique. Cette hormone rend
sa paroi perméable à l'eau et celleci est
dès lors extraite du tube parce que celuici traverse
la médullaire qui est hypertonique. L'hypertonicité
de la médullaire est créée et entretenue
grâce à un mécanisme de concentration par
contrecourant au niveau des anses de Henlé.
La prochaine leçon sera consacrée aux voies urinaires
 Reprenons le schéma général du néphron:
au glomérule fait suite la partie contournée
du tube proximal puis sa partie droite (en vert), le segment
grêle (en gris), la partie droite du tube distal
et sa partie contournée (en brun), s'abouchant à
un tube collecteur (en jaune) qui draine l'urine de plusieurs
néphrons vers l'orifice papillaire. Rappelons que la partie
droite du tube proximal, le segment grêle et la partie droite
du tube distal forment ensemble l'anse de Henlé.
Reprenons le schéma général du néphron:
au glomérule fait suite la partie contournée
du tube proximal puis sa partie droite (en vert), le segment
grêle (en gris), la partie droite du tube distal
et sa partie contournée (en brun), s'abouchant à
un tube collecteur (en jaune) qui draine l'urine de plusieurs
néphrons vers l'orifice papillaire. Rappelons que la partie
droite du tube proximal, le segment grêle et la partie droite
du tube distal forment ensemble l'anse de Henlé.


