Le système respiratoire (cours 2)
Le poumon comprend deux parties : la première, constituée
des bronches, bronchioles et canaux alvéolaires, purement
conductrice a été décrite dans la leçon
précédente. La deuxième, purement respiratoire,
est constituée d'alvéoles.
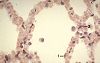 Les cavités arrondies ou polyédriques, visibles
ici, sont des cavités alvéolaires.
Leur nombre est estimé à 150 millions par poumons
et leur diamètre varie entre 100 micromètres à
l'expiration et 300 micromètres à l'inspiration.
Leur surface est évaluée à 80 m2. Leur paroi
ou septum interalvéolaire est mince. L'abondance des
globules rouges signe leur intense vascularisation capillaire.
Les septa sont limités de part et d'autre par un épithélium
pavimenteux qui leur est propre. Il est aussi aplati qu'un
endothélium. la distinction entre une cellule épithéliale
(1) et une cellule endothéliale (2) n'est pas toujours
aisée en miscroscopie optique. Quelques macrophages sont
libres dans la cavité alvéolaire.
Les cavités arrondies ou polyédriques, visibles
ici, sont des cavités alvéolaires.
Leur nombre est estimé à 150 millions par poumons
et leur diamètre varie entre 100 micromètres à
l'expiration et 300 micromètres à l'inspiration.
Leur surface est évaluée à 80 m2. Leur paroi
ou septum interalvéolaire est mince. L'abondance des
globules rouges signe leur intense vascularisation capillaire.
Les septa sont limités de part et d'autre par un épithélium
pavimenteux qui leur est propre. Il est aussi aplati qu'un
endothélium. la distinction entre une cellule épithéliale
(1) et une cellule endothéliale (2) n'est pas toujours
aisée en miscroscopie optique. Quelques macrophages sont
libres dans la cavité alvéolaire.
Les cellules septales proprement dites sont soit épithéliales
ou endothéliales. Les cellules épithéliales
sont pavimenteuses et appelées cellules alvéolaires
ou pneumocytes de type I. Les cellules épithéliales
plus volumineuses sont les cellules alvéolaires de type
II ou pneumocytes de type II. Dans l'interstitium, espace
entre l'épithélium et l'endothélium, on observe,
suivant les endroits, de rares fibroblastes, des macrophages,
des lymphocytes, des polynucléaires éosinophiles
et des mastocytes. A l'origine de chaque alvéole, les fibres
de collagène sont nombreuses et associées à
quelques fibres élastiques.
Voici plusieurs alvéoles
examinées dans une coupe épaisse d'un micromètre,
colorée au bleu de toluidine. Les cavités vasculaires
des septa sont dépourvues de globule rouge parce que le
poumon a été fixé par perfusion. Les capillaires
sont irréguliers et les noyaux endothéliaux (flèche)
font saillie dans leur lumière. L'épithélium
alvéolaire renferme des pneumocytes I, dont seuls
les noyaux sont apparents et bombent dans la cavité alvéolaire.
Les pneumocytes II sont plus volumineux et ont un cytoplasme
hétérogène.
Le cytoplasme des pneumocytes de type I
(P) contient des vésicules de micropinocytose, désignées
par des flèches, d'abondants ribosomes et quelques
lysosomes. La membrane basale de l'épithélium,
désignée par des têtes de flèche, est
nette à certains endroits. Ailleurs, elle est remplacée
par de petites fibres de collagène, souvent coupées
transversalement. Elle est séparée de la membrane
basale d'un capillaire par les prolongements de cellules interstitielles.
Dans la lumière du capillaire se trouve un lymphocyte (L).
Les pneumocytes de type II
sont habituellement nichés entre les capillaires mais peuvent
faire saillie dans la cavité alvéolaire. Leur répartition
est très variable. Ils font partie de l'épithélium
alvéolaire puisqu'ils sont unis aux pneumocytes de type
I par des complexes de jonction. Leur pôle apical est irrégulier.
Leur cytoplasme renferme de nombreux organites arrondis, les
corps lamellaires, vidés ici de leur contenu mais normalement
faits d'un empilement de membranes. Il contient aussi de nombreuses
mitochondries, des lysosomes et un abondant réticulum endoplasmique
rugueux. Les corps lamellaires sont la source du surfactant
alvéolaire.
 Le surfactant est un matériel lipoprotéique complexe,
comparable à un détergent. Il diminue la tension
superficielle du film liquide qui tapisse les cavités alvéolaires
ce qui empêche l'affaissement ou collapsus des alvéoles
lors de l'expiration. Il renferme douze fois plus de phospholipides
que de protéines. Les protéines les plus nombreuses
sont des glycoprotéines et les phospholipides les plus
importants sont des dérivés de la phosphatidylcholine
ou lécithine.
Le surfactant est un matériel lipoprotéique complexe,
comparable à un détergent. Il diminue la tension
superficielle du film liquide qui tapisse les cavités alvéolaires
ce qui empêche l'affaissement ou collapsus des alvéoles
lors de l'expiration. Il renferme douze fois plus de phospholipides
que de protéines. Les protéines les plus nombreuses
sont des glycoprotéines et les phospholipides les plus
importants sont des dérivés de la phosphatidylcholine
ou lécithine.
Une fixation adéquate permet de distinguer les deux phases
de l'enduit alvéolaire. L'épiphase est en
surface un film de densité variable, considéré
comme une couche monomoléculaire de phopholipides dépourvues
de protéines. L'hypophase est aqueuse. Elle contient
des protéines et occasionnellement des corps lamellaires.
L'importance des deux phases varie en fonction des mouvements
respiratoires.
Ce schéma
résume l'évolution des corps lamellaires
depuis leur synthèse jusqu'à leur inclusion dans
l'épiphase. Le pneumocyte de type II élabore des
corps lamellaires. Après fusion de leur membrane avec la
membrane cellulaire apicale, ils libèrent leur contenu
lamellaire dans l'hypophase. Là, leur sort est incertain.
Suivant les conditions, ils pourraient être transformés
en une forme active dans l'épiphase ou stockés dans
l'hypophase sous une forme structurée différente
de celle des corps lamellaires. Le stock de surfactant est important
et proportionnel au rythme respiratoire.
Les deux aspects de l'hypophase
représentés ici ont été photographiés
en microscopie électronique dans un repli de la paroi alvéolaire.
A gauche, l'hypophase est homogène et granulaire. A droite,
elle contient du surfactant de réserve composé de
lamelles empilées. Elles sont en majorité coupées
transversalement et forment un réseau de petits carrés.
Le pneumocyte de type II n'intervient pas uniquement dans
la synthèse et l'excrétion des phospholipides de
la partie active du surfactant. Il élabore aussi les glycoprotéines
de l'hypophase, peut régénérer l'épithélium
alvéolaire en se transformant en pneumocyte de type I et
intervient par sa micropinocytose dans les échanges d'eau
et d'électrolytes entre l'hypophase et l'interstitium.
Notons que l'hypophase n'est pas produite par les seuls pneumocytes
de type II. Une part de ses protéines proviennent des cellules
de Clara et son fluide est un transsudat à partir des
vaisseaux. Le surfactant n'est produit qu'au 7e mois de la vie
embryonnaire. Son insuffisance chez les nouveau-nés prématurés
est la cause d'une détresse respiratoire connue sous le
nom de maladie des membranes hyalines.
 Chaque septum interalvéolaire
possède un réseau de capillaire utilisé par
les deux alvéoles qu'il sépare. La proximité
de l'endothélium et de l'épithélium alvéolaire
est telle que la barrière alvéolo-capillaire
entre l'air et le sang est réduite à 0,1 ou 0,2
µm d'épaisseur. Une cellule endothéliale est
désignée par une flèche.
Chaque septum interalvéolaire
possède un réseau de capillaire utilisé par
les deux alvéoles qu'il sépare. La proximité
de l'endothélium et de l'épithélium alvéolaire
est telle que la barrière alvéolo-capillaire
entre l'air et le sang est réduite à 0,1 ou 0,2
µm d'épaisseur. Une cellule endothéliale est
désignée par une flèche.
Ces trois capillaires,
inclus dans un septum, font saillie dans une cavité alvéolaire
et contiennent des globules rouges. Un globule rouge se trouve
accidentellement dans la lumière alvéolaire suite
aux difficultés de la fixation. Le septum est typique.
Il possède d'un côté une paroi mince où
l'endothélium et l'épithélium ne sont séparés
que par une membrane basale commune. De l'autre côté,
la paroi est plus épaisse; l'endothélium et l'épithélium
sont séparés par un interstitium qui contient des
fibres de collagène. Cette alternance de zones minces
et épaisses se retrouve tout au long des septa interalvéolaires.
Une zone mince est ici fort
agrandie. La présence de globules rouges permet d'identifier
la partie vasculaire de la barrière alvéolo-capillaire.
Les deux membranes basales ont fusionné en une membrane
basale unique. L'épithélium alvéolaire
est très semblable à un endothélium, quoique
ce dernier ait plus de vésicules de micropinocytose. L'ultrastructure
de la barrière alvéolo-capillaire et du surfactant
qui la recouvre est particulièrement bien adaptée
aux échanges gazeux entre l'air et le sang. La fonction
principale de cette barrière est évidemment la captation
de l'O2 alvéolaire et l'élimination du CO2 sanguin.
Mais cette barrière peut intervenir dans la diffusion d'autres
substances volatiles comme l'eau, l'alcool, l'acétone,
les essences végétales, les gaz anesthésiques
ou toxiques. Leur élimination par le poumon ou leur diffusion
dans le sang dépend du gradient de pression qui
existe pour chacune d'elle entre le sang et l'alvéole et
de leur coefficient de solubilité.
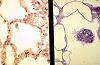 Dans les voies aériennes conductrices toutes les particules
inspirées dont le diamètre excède 3 micromètres
sont éliminées par l'appareil mucocilaire. Les plus
petites particules arrivent aux alvéoles où elles
sont phagocytées par les cellules à poussières.
Elles proviennent des monocytes sanguins et sont peu nombreuses
dans un poumon normal. On les identifie plus facilement lorsqu'elles
se trouvent dans la lumière alvéolaire. Leur noyau
est excentrique et leur cytoplasme riche en inclusions variées.
A droite, un macrophage a été coloré
au bleu de toluidine dans une coupe épaisse d'un micromètre;
son cytoplasme est hétérogène et son voile,
formé par un ensemble d'expansions cytoplasmiques, est
évident.
Dans les voies aériennes conductrices toutes les particules
inspirées dont le diamètre excède 3 micromètres
sont éliminées par l'appareil mucocilaire. Les plus
petites particules arrivent aux alvéoles où elles
sont phagocytées par les cellules à poussières.
Elles proviennent des monocytes sanguins et sont peu nombreuses
dans un poumon normal. On les identifie plus facilement lorsqu'elles
se trouvent dans la lumière alvéolaire. Leur noyau
est excentrique et leur cytoplasme riche en inclusions variées.
A droite, un macrophage a été coloré
au bleu de toluidine dans une coupe épaisse d'un micromètre;
son cytoplasme est hétérogène et son voile,
formé par un ensemble d'expansions cytoplasmiques, est
évident.
Cette cellule à poussières,
dont on ne voit pas le noyau, se déplace sur la paroi de
l'alvéole, grâce à un pseudopode irrégulier
et dépourvu d'organites. Normalement son efficacité
est telle qu'elle assure la stérilité de la surface
alvéolaire. L'évolution des particules phagocytées
dépend de leur nature et de leur nombre, mais aussi de
la voie empruntée par les macrophages pour quitter la surface
alvéolaire. Habituellement les cellules à poussières
sont prises en charge par l'appareil mucociliaire des voies
conductrices et sont expectorées.
Un certain nombre de cellules à poussières traversent
la paroi alvéolaire et gagnent le tissu interstitiel. Certaines
y restent; d'autres cheminent dans le chorion des bronchioles
où elles sont reprises par les voies lymphatiques et drainées
vers les ganglions du hile pulmonaire; d'autres enfin migrent
vers la plèvre. Si la concentration de particules non
dégradables, telles que des poussières minérales,
est excessive, les macrophages prolifèrent, absorbent ce
qu'ils peuvent et meurent. Les particules se retrouvent ainsi
dans les septa, la paroi des bronches et la plèvre.
Voici l'aspect macroscopique
d'un poumon normal à gauche et d'un poumon surchargé
de poussières de charbon, à droite. Ces dépôts
déclenchent une réaction inflammatoire chronique
qui entraîne une fibrose du parenchyme pulmonaire.
Le tissu fibreux imprégné de poussières est
noir et forme des nodules qui, au sommet du poumon, ont fusionné
en une masse volumineuse. Cette masse peut, en se nécrosant,
se creuser d'une cavité.
Les macrophages peuvent aussi passer d'une alvéole à
l'autre grâce aux pores interalvéolaires. La microscopie à balayage révèle ces pores
(IP) dont la taille, de l'ordre du micromètre, la forme
et le nombre sont variables. Leur présence semble importante
en cas d'obstruction bronchiolaire. Ils permettent l'égalisation
des pressions interalvéolaires et empêchent ainsi
l'affaissement des alvéoles, que l'on appelle collapsus
alvéolaire ou atélectasie. Quelques macrophages
(AP) au contour irrégulier sont accolés aux septa.
Un capillaire (Ca) et son érythrocyte (Er) sont visibles
dans un septum interalvéolaire.
La vascularisation sanguine des poumons dépend essentiellement
de la petite circulation, via les artères pulmonaires et
en partie de la grande, via les artères bronchiques.
 Les artères pulmonaires, issues du ventricule droit
ont un grand calibre et envoient le sang désoxygéné
aux poumons sous faible pression. Dans le parenchyme pulmonaire,
leurs ramifications suivent les bifurcations bronchiques et se
capillarisent au niveau des alvéoles. Les veines pulmonaires
recueillent le sang oxygéné des capillaires
alvéolaires et l'envoient vers l'oreillette gauche. La
circulation pulmonaire assure les échanges gazeux entre
l'air et le sang.
Les artères pulmonaires, issues du ventricule droit
ont un grand calibre et envoient le sang désoxygéné
aux poumons sous faible pression. Dans le parenchyme pulmonaire,
leurs ramifications suivent les bifurcations bronchiques et se
capillarisent au niveau des alvéoles. Les veines pulmonaires
recueillent le sang oxygéné des capillaires
alvéolaires et l'envoient vers l'oreillette gauche. La
circulation pulmonaire assure les échanges gazeux entre
l'air et le sang.
Les artères bronchiques ont un petit calibre et
proviennent de l'aorte. Elles amènent au poumon du sang
oxygéné sous pression élevée.
Elles se trouvent dans la paroi bronchique, où elles se
ramifient progressivement. Leur sang est évacué
en partie par des veines bronchiques vers la veine cave
supérieure mais peut également rejoindre les veines
pulmonaires. La circulation bronchique a une fonction trophique.
Entre les deux circulations existent plusieurs types d'anastomoses
qui seront décrits plus loin.
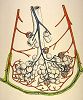
Les artères pulmonaires, en bleu dans ce schéma,
suivent le trajet des bronches. Leurs artérioles
respiratoires longent les bronchioles terminales puis les bronchioles
respiratoires jusqu'aux canaux alvéolaires où elles
se capillarisent. Tous les capillaires alvéolaires proviennent
de cette circulation. Leur sang oxygéné ainsi que
celui de la plèvre est repris par des veinules,
représentées en rouge dans ce schéma, puis
par des veines qui cheminent indépendamment des bronchioles
et des bronches. A la périphérie du poumon,
elles sont situées dans des septa conjonctifs plus ou moins
importants. Seules les larges veines pulmonaires, non représentées
ici, rejoignent l'arbre bronchique au niveau des grosses bronches.
La paroi des artères et des artérioles pulmonaires
est mince parce que la pression qui y règne est
basse. Pour les distinguer des veines, il faudra donc considérer
non seulement leur structure, mais aussi leur localisation
proche des voies aériennes conductrices. L'association
des bronches et des artères pulmonaires est particulièrement
constante dans l'espèce humaine où les deux
organes à chaque embranchement ont approximativement le
même diamètre. Elle explique l'image en lunettes
des radiologues qui voient côte à côte deux
petites surfaces rondes de même taille. L'une est sombre,
c'est la coupe transversale d'une bronche, l'autre est claire,
c'est la coupe transversale d'une artère pulmonaire. Les
artères pulmonaires et la plupart de leurs ramifications
sont élastiques. Lorsque leur diamètre est
inférieur à 1 mm, elles deviennent musculeuses.
L'artère pulmonaire,
observée ici, est localisée à proximité
d'une bronche segmentaire dont on ne voit pas les nodules
cartilagineux. Son calibre est assez important. Son adventice
mince et dense la relie au tissu conjonctif péribronchique.
Dans sa média,
la proportion des cellules musculaires lisses est plus
importante que celle des lames élastiques, parce que le
poumon a été prélevé chez un rat.
Les lames élastiques sont les quelques fines lignes bleuâtres
parallèles qui séparent les nombreuses cellules
musculaires lisses.
Cette artériole pulmonaire
est située en dehors d'une bronchiole terminale, mais y
est reliée par son adventice. Sa média, très
mince, est réduite à quelques couches de cellules
musculaires lisses.
Les artérioles pulmonaires se démunissent progressivement
de leurs cellules musculaires et se capillarisent dès le
début des canaux alvéolaires. La transition artériole-capillaire
est dépourvue de sphincter précapillaire. Les capillaires
sont désignés par des flèches.
Le sang oxygéné des alvéoles ainsi que le
sang en provenance de la plèvre se jette dans des veinules
pulmonaires. Dans une coupe colorée selon une méthode
trichromique, la veinule pulmonaire
est typique. Elle est entourée d'alvéoles et
chemine indépendamment des bronchioles dans le parenchyme
pulmonaire. Son adventice mince est limitée à quelques
fines fibres bleuâtres de collagène.
Ici se rejoignent plusieurs veinules
non loin d'une bronche segmentaire. La veine qui en résulte
possède une gaine conjonctive plus épaisse. Dans
l'espèce humaine, dès que leur diamètre excède
100 µ, elles s'enrichissent en cellules musculaires lisses.
Leur localisation à l'écart des bronchioles,
l'absence de lame élastique et la minceur de leur couche
musculeuse permettent de les distinguer des artères pulmonaires.
Cette grande cavité allongée, remplie de sang, est
celle d'une veine pulmonaire;
elle a rejoint l'arbre bronchique au niveau d'une bronche segmentaire
et sa couche fibreuse externe la relie à la paroi bronchique.
Comparez cette veine aux autres vaisseaux de cette préparation.
Celui qui est désigné par une flèche est
une veinule qui chemine à l'écart
de l'arbre bronchique. Celui qui est désigné par
une astérisque, est accolé à la bronche
et son calibre est plus petit que celui de la veine; il s'agit
d'une artériole pulmonaire. Enfin, le dernier, désigné
par une tête de flèche, se trouve dans la paroi
de la bronche, c'est une artériole bronchique.
La circulation bronchique est d'origine aortique et alimente
les voies aériennes conductrices, les gros vaisseaux et
la plèvre. Ses artères musculeuses sont dans
le tissu conjonctif des bronches. Il n'existe plus de circulation
bronchique au niveau des dernières bronchioles respiratoires.
Cette artériole bronchique
est dans le chorion de la bronche. Sa média ne comprend
qu'une seule couche de cellules musculaires lisses. Ses capillaires
sont destinés aux glandes et aux muscles. Le sang bronchique
est drainé par des veines dont la localisation est identique
à celle des artères et par les veines pulmonaires.
Parmi les anastomoses entre les circulations pulmonaire et bronchique,
on distingue les anastomoses artério-artérielles,
artério-veineuses, veino-veineuses et intercapillaires.
Toutes ces anastomoses sauf les veino-veineuses ne deviennent
fonctionnelles qu'en cas de lésion pulmonaire.
 La circulation lymphatique pulmonaire est bien développée.
Elle comprend deux réseaux quasi indépendants: le
superficiel est destiné à la plèvre
et le profond au parenchyme pulmonaire. Ces deux réseaux
se rassemblent près du hile pulmonaire où ils sont
drainés par les ganglions hilaires, puis par les ganglions
trachéo-bronchiques. Chaque réseau renferme des
capillaires lymphatiques très perméables et des
vaisseaux collecteurs plus larges et relativement imperméables.
La circulation lymphatique pulmonaire est bien développée.
Elle comprend deux réseaux quasi indépendants: le
superficiel est destiné à la plèvre
et le profond au parenchyme pulmonaire. Ces deux réseaux
se rassemblent près du hile pulmonaire où ils sont
drainés par les ganglions hilaires, puis par les ganglions
trachéo-bronchiques. Chaque réseau renferme des
capillaires lymphatiques très perméables et des
vaisseaux collecteurs plus larges et relativement imperméables.
Les vaisseaux superficiels sont larges et forment un réseau
à mailles polyédriques où aboutissent de
nombreux capillaires qui débutent par un cul-de-sac. Le
réseau lymphatique superficiel est bien développé
chez l'enfant.
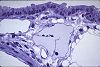
Le réseau profond est composé de lymphatiques péribronchiques
qui suivent le trajet des voies respiratoires conductrices jusqu'aux
bronchioles terminales. Le vaisseau lymphatique central muni
de deux valvules est ici situé entre une bronchiole
terminale, une veinule bronchique, une artériole pulmonaire
et une cavité alvéolaire. Les bronchioles respiratoires,
les canaux alvéolaires et les septa interalvéolaires
sont, quant à eux dépourvus de vaisseaux lymphatiques.
Leur liquide interstitiel s'écoule jusqu'aux premiers capillaires
lymphatiques, localisés à la jonction des septa
interalvéolaires et du tissu conjonctif périvasculaire,
péribronchique ou pleural.
L'innervation pulmonaire comprend des fibres réceptrices,
des fibres effectrices parasympathiques et des fibres effectrices
orthosympathiques. Les terminaisons des fibres réceptrices
se trouvent dans le chorion et dans l'épithélium
de l'arbre bronchique et des alvéoles. Ces fibres aboutissent
au système nerveux central via le nerf vague. Les
fibres parasympathiques proviennent du nerf vague; leurs
terminaisons sont cholinergiques et provoquent la contraction
des muscles bronchiques et bronchiolaires, la sécrétion
glandulaire et la vasodilatation. Les fibres orthosympathiques
proviennent des premiers ganglions prévertébraux
thoraciques; leurs terminaisons sont adrénergiques.
Leur stimulation relâche les muscles bronchiques et bronchiolaires,
inhibe la sécrétion et provoque une vasoconstriction.
La plèvre est une membrane séreuse constituée
de deux feuillets en continuité au niveau du hile pulmonaire.
Le feuillet pariétal est appliqué contre
la cage thoracique et le feuillet viscéral est accolé
à la surface pulmonaire. Ils sont séparés
par la cavité pleurale. Celle-ci est quasi virtuelle et
ne contient normalement qu'une faible quantité de liquide
et quelques globules blancs. Il y règne une pression
négative qui permet l'expansion pulmonaire lors de
l'inspiration.
Les deux feuillets pleuraux ont la même structure. Ils comprennent
un mésothélium et un chorion mince non vascularisé
ainsi qu'une couche profonde fibro-élastique. Dans l'espèce
humaine, la plèvre est rattachée à la paroi
des alvéoles les plus superficielles par le tissu sous-pleural,
composé de deux bandes conjonctives. L'externe est lâche
et bien vascularisé; l'interne est riche en fibres élastiques.
L'organisation complexe de la plèvre humaine n'apparaît
pas dans cette coupe de poumon de rat où
seul le mésothélium est typique. Les cellules de
cet épithélium pavimenteux simple ont de nombreuses
expansions filiformes qui plongent dans la cavité pleurale.
Le chorion est représenté par une mince couche claire.
La plèvre humaine est sillonnée de lignes qui dessinent
un réseau en nids d'abeille. Elles sont particulièrement
nettes dans cette vue de face d'un poumon de personne âgée.
En effet, elles sont soulignées par l'accumulation, au
cours des années, de macrophages surchargés
par des particules de carbone en provenance de l'air inhalé.
Chaque nid d'abeille est la base d'un lobule.
 Le lobule pulmonaire
peut être considéré comme l'unité
morphologique du poumon. Il a la forme d'une pyramide tronquée
dont le sommet est orienté vers le hile pulmonaire et dont
la base est appliquée contre la plèvre. Il est entièrement
délimité par des septa conjonctifs riches en fibres
élastiques. Il comprend une à trois bronchioles
terminales et leurs ramifications. Sa taille est donc variable.
Dans ce lobule, on a représenté la subdivision d'une
bronchiole terminale en trois générations de bronchioles
respiratoires comme elle se fait dans l'espèce humaine.
L'artère pulmonaire est en bleu parce qu'elle amène
le sang désoxygéné; elle suit le trajet des
bronches jusqu'aux canaux alvéolaires et se capillarise
dans les septa interalvéolaires. Le sang oxygéné,
représenté en rouge, est repris par les veinules
pulmonaires qui se rassemblent dans les cloisons conjonctives.
Le lobule pulmonaire
peut être considéré comme l'unité
morphologique du poumon. Il a la forme d'une pyramide tronquée
dont le sommet est orienté vers le hile pulmonaire et dont
la base est appliquée contre la plèvre. Il est entièrement
délimité par des septa conjonctifs riches en fibres
élastiques. Il comprend une à trois bronchioles
terminales et leurs ramifications. Sa taille est donc variable.
Dans ce lobule, on a représenté la subdivision d'une
bronchiole terminale en trois générations de bronchioles
respiratoires comme elle se fait dans l'espèce humaine.
L'artère pulmonaire est en bleu parce qu'elle amène
le sang désoxygéné; elle suit le trajet des
bronches jusqu'aux canaux alvéolaires et se capillarise
dans les septa interalvéolaires. Le sang oxygéné,
représenté en rouge, est repris par les veinules
pulmonaires qui se rassemblent dans les cloisons conjonctives.
A côté de cette subdivision, basée sur la
distribution du tissu conjonctif, on a imaginé d'autres
subdivisions. On appelle acinus pulmonaire le territoire d'une
seule bronchiole terminale; sa partie périphérique
est parfois isolée par des septa incomplets. On appelle
lobule primaire le territoire d'une bronchiole respiratoire.
 Les cavités arrondies ou polyédriques, visibles
ici, sont des cavités alvéolaires.
Leur nombre est estimé à 150 millions par poumons
et leur diamètre varie entre 100 micromètres à
l'expiration et 300 micromètres à l'inspiration.
Leur surface est évaluée à 80 m2. Leur paroi
ou septum interalvéolaire est mince. L'abondance des
globules rouges signe leur intense vascularisation capillaire.
Les septa sont limités de part et d'autre par un épithélium
pavimenteux qui leur est propre. Il est aussi aplati qu'un
endothélium. la distinction entre une cellule épithéliale
(1) et une cellule endothéliale (2) n'est pas toujours
aisée en miscroscopie optique. Quelques macrophages sont
libres dans la cavité alvéolaire.
Les cavités arrondies ou polyédriques, visibles
ici, sont des cavités alvéolaires.
Leur nombre est estimé à 150 millions par poumons
et leur diamètre varie entre 100 micromètres à
l'expiration et 300 micromètres à l'inspiration.
Leur surface est évaluée à 80 m2. Leur paroi
ou septum interalvéolaire est mince. L'abondance des
globules rouges signe leur intense vascularisation capillaire.
Les septa sont limités de part et d'autre par un épithélium
pavimenteux qui leur est propre. Il est aussi aplati qu'un
endothélium. la distinction entre une cellule épithéliale
(1) et une cellule endothéliale (2) n'est pas toujours
aisée en miscroscopie optique. Quelques macrophages sont
libres dans la cavité alvéolaire.



