Les glandes endocrines (cours 4)
Les glandes impliquées dans la régulation du métabolisme
phosphocalcique sont l'ensemble des cellules claires ou parafolliculaires
de la thyroïde, et les parathyroïdes.
 Les cellules C ou claires
ou parafolliculaires sont volumineuses, leur cytoplasme est plus
clair que celui des cellules folliculaires, d'où leur nom.
Leur noyau est pâle et ovoïde. Elles sont enchâssées
dans l'épithélium folliculaire, mais ne viennent
jamais en contact avec le colloïde. Elles peuvent aussi former
des amas dans le chorion.
Les cellules C ou claires
ou parafolliculaires sont volumineuses, leur cytoplasme est plus
clair que celui des cellules folliculaires, d'où leur nom.
Leur noyau est pâle et ovoïde. Elles sont enchâssées
dans l'épithélium folliculaire, mais ne viennent
jamais en contact avec le colloïde. Elles peuvent aussi former
des amas dans le chorion.
Dans une coupe semi-fine, on les reconnaît aisément.
En voici quelques-unes indiquées par des flèches.
Dans les préparations histologiques habituelles, les cellules C
sont difficilement reconnaissables. Ici, chez ce jeune
chien, elles sont plus volumineuses et leur cytoplasme n'est pas
coloré. Une d'entre elles est indiquée par une flèche.
Les grains de sécrétion
sont petits et distribués dans tout le cytoplasme. Ils
sont ronds ou ovoïdes, et leur matrice est dense.
Comme nous l'avons déjà mentionné, les cellules
C dérivent des crêtes neurales rhombencéphaliques
et migrent avec les corps ultimobranchiaux avant de coloniser
la thyroïde. Leur origine embryonnaire et leurs propriétés
histochimiques les classent dans les cellules du système
APUD. Leurs grains contiennent surtout de la calcitonine,
peptide de 32 acides aminés, mais aussi de la sérotonine
et de la somatostatine. Le rôle de la calcitonine
est de diminuer la calcémie en stimulant les ostéoblastes,
et donc l'ostéosynthèse, et en favorisant
l'excrétion rénale des ions calcium et phosphates.
L'action de la calcitonine sur l'absorption intestinale du calcium
ionisé est complexe et mal connue.
 Les parathyroïdes,
chez l'homme, sont habituellement au nombre de quatre. Leur taille
normale varie entre 3 et 8 mm en longueur, entre 2 et 5 mm en
largeur et entre 0,5 et 2 mm en épaisseur. Le poids total
du parenchyme parathyroïdien est inférieur à
1 g. Elles sont situées dans la capsule de la thyroïde
ou en sont séparées par du tissu conjonctif lâche.
Sur ce schéma, cette localisation normale a été
représentée en traits pleins. Les localisations
ectopiques, dues à un trouble de leur migration embryonnaire,
ont été représentées en pointillé.
En outre, des variations de taille et de nombre sont fréquentes.
Les parathyroïdes,
chez l'homme, sont habituellement au nombre de quatre. Leur taille
normale varie entre 3 et 8 mm en longueur, entre 2 et 5 mm en
largeur et entre 0,5 et 2 mm en épaisseur. Le poids total
du parenchyme parathyroïdien est inférieur à
1 g. Elles sont situées dans la capsule de la thyroïde
ou en sont séparées par du tissu conjonctif lâche.
Sur ce schéma, cette localisation normale a été
représentée en traits pleins. Les localisations
ectopiques, dues à un trouble de leur migration embryonnaire,
ont été représentées en pointillé.
En outre, des variations de taille et de nombre sont fréquentes.
La parathyroïde
est limitée par une capsule conjonctive. Chez le jeune
individu, son parenchyme est composé d'un type unique
de petites cellules disposées en cordons anastomosés,
entre lesquels se trouvent des vaisseaux et quelques adipocytes.
Les cellules glandulaires, dites cellules principales, ont un
cytoplasme clair ou granulaire.
Chez l'adulte, la glande est fort différente, parce qu'elle
a subi une involution adipeuse.
Le parenchyme est réduit et le volume du tissu adipeux
peut atteindre 60 à 70% de l'organe. Outre les cellules
principales, un autre type cellulaire se développe dès
la puberté: les cellules oxyphiles; elles sont plus
volumineuses et leur cytoplasme est éosinophile.
Voici, à fort grossissement la différence entre
les cellules principales et une cellule oxyphile indiquée
par une flèche, dans une coupe de parathyroïde humaine
colorée à l'hémalun-éosine-safran.
La cellule principale est petite, de 4 à 8 µm
de diamètre; son noyau est rond. Son cytoplasme est clair,
il peut même paraître vacuolaire à cause des
larges plages de glycogène qu'il contient parfois et qui
ont été extraites au cours de la préparation.
Elle sécrète la parathormone.
La cellule oxyphile est plus volumineuse, de 8 à
10 µm de diamètre, son noyau est petit, dense et central,
parfois en voie de pycnose. Le cytoplasme est acidophile et granulaire,
à cause de ses très nombreuses mitochondries. Le
rôle de ces cellules n'est pas connu. Pour certains, elles
seraient en voie de dégénérescence; cependant,
leur très grand nombre dans l'adénome parathyroïdien
suggère qu'elles ont un rôle dans la synthèse
de la parathormone ou dans la régulation de sa sécrétion.
Le cycle de sécrétion dans la cellule principale
est bien particulier. Lorsque la cellule est au repos, son cytoplasme
est clair et contient de larges plages de glycogène, très
peu de réticulum endoplasmique rugueux et un appareil de
Golgi fortement réduit. Lorsque la cellule est en phase
sécrétoire, son cytoplasme est plus foncé,
le glycogène ayant disparu, puis le réticulum et
l'appareil de Golgi se développant progressivement. Enfin,
des vésicules de condensation et des grains immatures,
au contenu peu dense, se forment dans le cytoplasme.
Voici les cellules principales
à des stades différents de leur activité.
Les unes sont au repos et leur cytoplasme semble pratiquement
vide. D'autres, indiquées par des flèches, sont
en phase sécrétoire et leur cytoplasme est plus
développé et granulaire.
Au début de la phase sécrétoire,
le réticulum endoplasmique rugueux est développé
et prend fréquemment un aspect spiralé, l'appareil
de Golgi est composé de nombreux saccules dont certains
contiennent un matériel granulaire qui est le précurseur
des hormones. Des vésicules de condensation, reconnaissables
à leur grande taille et à leur contenu modérément
dense, sont également visibles et indiquées par
des flèches.
Les parathyroïdes dérivent de l'endoderme des
troisièmes et quatrièmes fentes branchiales. Elles
sécrètent la parathormone, peptide de 84
acides aminés dont les 34 premiers possèdent une
activité biologique comparable à la molécule
entière. Son action est hypercalcémiante.
Ce schéma
résume les rôles respectifs de la calcitonine
(flèches rouges) et de la parathormone (flèches
bleues) dans le métabolisme phosphocalcique.
La concentration du calcium, et en particulier celle du calcium
ionisé, dans le milieu extracellulaire ne peut varier
que dans des limites très étroites. Plusieurs contrôles
concourent à l'y maintenir.
L'absorption du calcium au niveau du tube digestif augmente sous
l'influence de la parathormone, dont l'activité dépend
en partie de la vitamine D. Le squelette représente une
réserve énorme de calcium, qui y est essentiellement
sous forme de phosphates. Selon les besoins, les os
incorporent du calcium sous l'effet de la calcitonine qui
stimule les ostéoblastes et donc l'ostéogenèse.
Le squelette en libère sous l'effet de la parathormone
qui stimule l'activité des ostéoclastes et augmente
leur nombre. Les deux hormones, enfin, agissent sur les reins
qui participent à la régulation de la calcémie.
La calcitonine augmente la perte urinaire en ions calcium
et phosphates tandis que la parathormone favorise la réabsorption
tubulaire du calcium ionisé.
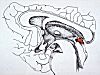 Chez l'homme, l'épiphyse
ou glande pinéale est un petit organe conique, de
7 à 10 mm de haut et pesant 100 à 200 mg. Elle est
située dans le toit du troisième ventricule, sous
la portion postérieure du corps calleux et dans la gouttière
formée par les tubercules quadrijumeaux antérieurs.
Chez l'homme, l'épiphyse
ou glande pinéale est un petit organe conique, de
7 à 10 mm de haut et pesant 100 à 200 mg. Elle est
située dans le toit du troisième ventricule, sous
la portion postérieure du corps calleux et dans la gouttière
formée par les tubercules quadrijumeaux antérieurs.
Chez le rat, le corps calleux et les hémisphères
cérébraux sont moins développés, l'épiphyse
est donc située immédiatement en arrière
du lobe occipital et en avant du cervelet. A ce faible grossissement,
l'épiphyse a l'aspect d'une masse cellulaire compacte,
enveloppée d'une fine capsule contenant des vaisseaux.
 Cette capsule est
fibreuse, elle provient d'un épaississement de la pie-mère.
Des septa s'en détachent et dissocient le parenchyme glandulaire;
ils contiennent des fibres nerveuses et des vaisseaux. La base
de l'épiphyse est dirigée vers le troisième
ventricule.
Cette capsule est
fibreuse, elle provient d'un épaississement de la pie-mère.
Des septa s'en détachent et dissocient le parenchyme glandulaire;
ils contiennent des fibres nerveuses et des vaisseaux. La base
de l'épiphyse est dirigée vers le troisième
ventricule.
Pour comprendre la structure et la fonction des cellules de la
glande pinéale, il est nécessaire de revoir rapidement
l'histologie et la fonction de cet organe chez des animaux inférieurs.
Chez le lézard,
l'épiphyse a la forme d'un sac et est reliée par
un nerf à un oeil rudimentaire et médian
qui possède un segment antérieur, translucide et
un segment postérieur, photorécepteur. Les informations
lumineuses recueillies par cet organe médian sont transmises
à l'épiphyse par le nerf pinéal.
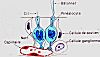 Chez la grenouille, l'épiphyse a toujours la forme d'un
sac. Sa paroi comprend des cellules de soutien, des cellules
ganglionnaires, dont le rôle n'est pas connu, et des
pinéalocytes, analogues aux cellules photosensibles
de l'organe médian des lézards. Les pinéalocytes
ont un corps cellulaire globuleux et deux prolongements: l'un,
photosensible, est l'équivalent du bâtonnet
de la rétine. Son ultrastructure complexe n'a pas été
représentée sur cette image. Sa portion proximale
est remplie de petites vésicules et de mitochondries et
sa portion distale est constituée de très nombreux
replis de la membrane plasmique se disposant comme les dents d'un
peigne. L'autre prolongement est l'équivalent de l'axone
d'une cellule rétinienne, mais, au lieu de faire synapse
avec une autre cellule nerveuse, il se termine par une dilatation
ampullaire à proximité de petits capillaires fenestrés.
Comme les neurites des cellules nerveuses, les prolongements des
pinéalocytes contiennent de très nombreux microtubules.
Chez la grenouille, l'épiphyse a toujours la forme d'un
sac. Sa paroi comprend des cellules de soutien, des cellules
ganglionnaires, dont le rôle n'est pas connu, et des
pinéalocytes, analogues aux cellules photosensibles
de l'organe médian des lézards. Les pinéalocytes
ont un corps cellulaire globuleux et deux prolongements: l'un,
photosensible, est l'équivalent du bâtonnet
de la rétine. Son ultrastructure complexe n'a pas été
représentée sur cette image. Sa portion proximale
est remplie de petites vésicules et de mitochondries et
sa portion distale est constituée de très nombreux
replis de la membrane plasmique se disposant comme les dents d'un
peigne. L'autre prolongement est l'équivalent de l'axone
d'une cellule rétinienne, mais, au lieu de faire synapse
avec une autre cellule nerveuse, il se termine par une dilatation
ampullaire à proximité de petits capillaires fenestrés.
Comme les neurites des cellules nerveuses, les prolongements des
pinéalocytes contiennent de très nombreux microtubules.
Les pinéalocytes des mammifères
dérivent directement des cellules photoréceptrices
des animaux inférieurs. Ils possèdent également
deux prolongements. Celui qui correspond au prolongement photosensible
est devenu atrophique et ne contient que des petites vésicules
et de nombreuses mitochondries. Par contre l'autre prolongement
s'est développé et est devenu neurosécréteur:
son extrémité distale est remplie de vésicules
ou de grains de sécrétion. Il contient parfois des
gouttelettes lipidiques.
Le corps cellulaire est globuleux, le noyau est échancré
et le cytoplasme abondant contient tous les organites nécessaires
à une synthèse hormonale de type protéique.
On y trouve en outre la bandelette synaptique qui n'existe
que dans un seul autre type cellulaire: le bâtonnet de la
rétine. Elle est composée d'une association de microtubules
entourés de petites vésicules. Des fibres nerveuses
nues, originaires du système sympathique cervical courent
le long des pinéalocytes. Enfin, des cellules allongées,
dites de soutien, sont accolées au corps et aux prolongements
des pinéalocytes.
Voici une épiphyse de rat
en coupe semi-fine. L'animal a été perfusé
pour mieux séparer les différents constituants glandulaires.
Les pinéalocytes ont un volumineux noyau pâle. Leur
cytoplasme contient des gouttelettes lipidiques colorées
en vert. Les cellules s'associent en îlots séparés
par des septa contenant quelques cellules de soutien, des fibroblastes
et des capillaires. Au sein de ces îlots se trouvent de
petits espaces intercellulaires qui ne contiennent pas de vaisseaux
mais parfois des prolongements de pinéalocytes (flèche).
Le prolongement non sécréteur
du pinéalocyte contient des mitochondries allongées
et tassées les unes contre les autres, quelques vésicules
et de nombreux microtubules.
La terminaison sécrétrice
d'un pinéalocyte est ici accolée à une autre
cellule et contient de nombreux grains denses, des mitochondries
et quelques gouttelettes lipidiques.
Voici une cellule de soutien;
elle est grêle et son noyau est ovoïde. Le cytoplasme
émet de fins prolongements qui longent les cellules.
L'épiphyse humaine contient aussi des psammomes,
masses arrondies ou polycycliques calcifiées qui,
colorées à l'hémalun-éosine-safran,
ont une couleur rouge pourpre. Ces calcifications apparaissent
à la puberté; leur nombre et leur taille augmentent
avec l'âge. Leur origine et leur rôle sont inconnus.
Encore récemment, on utilisait ces calcifications comme
repères en radiologie: leur déplacement latéral,
visible sur une radiographie de face, est le signe d'un
processus expansif localisé du côté opposé
au déplacement.
L'épiphyse sécrète une hormone aminée,
la mélatonine ou 5-méthoxy-N-acétyl-sérotonine,
synthétisée à partir de la sérotonine.
Son effet sur la régulation du développement et
du fonctionnement des gonades est le mieux connu. La mélatonine
induit une régression de celles-ci, en inhibant
la sécrétion de la LH et de la FSH et en réduisant
la sécrétion de la prolactine. La mélatonine
a aussi un effet anti-MSH évident sur la peau des
batraciens, ce qui explique son nom. Elle intervient également
dans la mue de nombreux animaux.
L'épiphyse sécrète aussi d'autres substances
aminées et de petites protéines dont les fonctions
sont mal connues: elles interviendraient, entre autre, dans la
régulation de la motricité et du sommeil.
L'aspect le plus remarquable de la physiologie épiphysaire
est le rythme de sa sécrétion et la régulation
de ce rythme par la lumière. La sécrétion
de la mélatonine est stimulée par le système
orthosympathique à partir d'une "horloge biologique
interne" située dans l'hypothalamus. Cette horloge
transmet ses stimuli à l'épiphyse via le mésencéphale,
la corne intermédio-latérale de la moelle cervicale,
le ganglion cervical supérieur et un nerf.
La lumière est perçue chez les lézards par
l'oeil rudimentaire médian et les stimuli qu'elle
provoque aboutissent directement par le nerf pinéal
à l'épiphyse, siège de l'"horloge biologique".
Chez les mammifères, la lumière est perçue
par les yeux et les stimuli qu'elle provoque aboutissent
à l'hypothalamus et bloquent l'effet stimulant de l'"horloge
biologique".
L'horloge biologique interne modulée par la lumière
règle la sécrétion de mélatonine en
fonction d'un rythme circadien et d'un rythme saisonnier.
En effet, le raccourcissement de la journée induit une
augmentation de la sécrétion nocturne de la mélatonine,
qui provoque la régression des organes génitaux,
une modification du comportement sexuel et la mue saisonnière
chez de nombreux animaux. Chez l'homme, la régulation est
plus complexe, mais la présence des rythmes circadien et
saisonnier a été démontrée.
 Au cours de la gestation, l'équilibre endocrinien maternel
est profondément modifié par de nouvelles structures
endocrines: le corps jaune de grossesse, le cortex foetal
surrénalien et le placenta. Leur description
détaillée sera vue avec le système génital;
nous nous limiterons à la description des cellules dont
les caractères généraux sont ceux des cellules
endocrines sécrétant des protéines ou des
lipides.
Au cours de la gestation, l'équilibre endocrinien maternel
est profondément modifié par de nouvelles structures
endocrines: le corps jaune de grossesse, le cortex foetal
surrénalien et le placenta. Leur description
détaillée sera vue avec le système génital;
nous nous limiterons à la description des cellules dont
les caractères généraux sont ceux des cellules
endocrines sécrétant des protéines ou des
lipides.
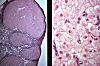
Le corps jaune de grossesse,
représenté à faible grossissement dans l'image
de gauche, est beaucoup plus volumineux que le corps jaune qui
se développe au cours de la seconde partie d'un cycle sans
fécondation. Il dérive cependant de celui-ci. Il
est formé de grandes cellules au cytoplasme rempli de vésicules
lipidiques, mais, chose particulière, les gouttelettes
d'une même cellule sont de taille variable, contrairement
à ce que l'on voit dans les autres glandes qui sécrètent
des stéroïdes. Le corps jaune de grossesse sécrète
surtout de la progestérone.
Le cortex foetal surrénalien, improprement appelé
zone X, participe à la synthèse des oestrogènes.
Le cholestérol y subit une première transformation;
le produit de cette transformation est sécrété
dans le sang foetal et arrive au placenta où la synthèse
hormonale se termine.
L'étude du rôle respectif de la progestérone
et des oestrogènes au cours de la gestation relève
de la physiologie.
Certaines cellules placentaires synthétisent des
hormones de nature protéique dont les principales sont
l'HCG (Human Chorionic Gonadotrophin) et l'HPL (Human
Placental Lactogen) . Elles possèdent donc l'ultrastructure
caractéristique des cellules sécrétant des
peptides dont la détection se fait en utilisant des techniques
immunocytochimiques. Voici à titre d'exemple, la détection
de l'HCG dans une villosité placentaire,
selon la technique peroxydase anti-peroxydase décrite dans
la première leçon. Les cellules qui contiennent
cette hormone sont remplies d'une substance brunâtre, produit
de la réaction histochimique.
 Les reins produisent de nombreuses hormones dont la principale
est la rénine qui, avec l'angiotensine forme le
système rénine-angiotensine. Il sécrète
en outre l'érythropoïétine et certaines
prostaglandines. La microanatomie, l'ultrastructure et
l'embryogenèse des reins sont vus avec le système
urinaire.
Les reins produisent de nombreuses hormones dont la principale
est la rénine qui, avec l'angiotensine forme le
système rénine-angiotensine. Il sécrète
en outre l'érythropoïétine et certaines
prostaglandines. La microanatomie, l'ultrastructure et
l'embryogenèse des reins sont vus avec le système
urinaire.
La rénine est synthétisée et sécrétée
par les cellules de l'appareil juxta-glomérulaire.
Celui-ci est composé des cellules de la paroi de l'artériole
afférente du néphron (1), de la macula densa,
portion spécialisée du tube contourné distal
(2) et du coussinet polaire (3). Ce dernier est situé
dans l'espace limité par les artérioles afférente
et efférente (4), la macula densa (2) et le glomérule
(5).
Les cellules du coussinet polaire sont de deux types. Les unes
sont des cellules mésangiales extra-glomérulaires,
dont le cytoplasme est clair. Les autres, responsables de la sécrétion
de rénine, sont des cellules musculaires lisses
très spécialisées de l'artériole afférente:
elles sont polygonales, contiennent des grains de sécrétion
et sont en étroite relation avec l'intima de l'artère
d'une part, et avec la macula densa d'autre part. Les cellules
de la macula densa ont une polarité inversée et
dirigée vers les cellules du coussinet polaire. Les relations
exactes entre ces deux cellules ne sont pas connues mais à
cet endroit, la membrane basale du tube contourné est plus
mince qu'ailleurs. Des terminaisons adrénergiques
(6) sont en contact étroit avec l'artériole afférente.
Voici la coupe d'un corpuscule rénal.
On reconnaît dans la partie centrale la masse des capillaires
appartenant au glomérule et séparée du feuillet
pariétal de la capsule de Bowman par un espace clair. Au-dessus
du glomérule se trouve la portion différentiée
du tube contourné distal. Les cellules de ce tube en rapport
avec les capillaires sont cylindriques; ensemble, elles constituent
la macula densa. A droite du corpuscule, on reconnaît
l'artériole afférente dont la lumière est
limitée par un endothélium. Les cellules musculaires
de sa média sont modifiées au voisinage de la macula
densa. Ces cellules appartiennent au coussinet polaire
qui s'insinue en formant un coin entre le corpuscule et le tube
contourné.
La rénine n'est pas une hormone au sens propre du
terme parce qu'elle n'agit pas sur une cellule cible. Elle est
une enzyme protéolytique qui agit dans le rein et
dans le plasma sur l'angiotensinogène, globuline
synthétisée par le foie. La rénine libère,
à partir de l'angiotensinogène, un décapeptide,
l'angiotensine I qui ne devient actif qu'après sa
transformation en un octapeptide, l'angiotensine II, sous
l'influence d'une enzyme de conversion, présente dans le
plasma. L'angiotensine II est essentiellement hypertensive.
Son métabolisme est très rapide et sa 1/2 vie plasmatique
est de 90 secondes. Elle est transformée en résidus
peptidiques inactifs sous l'effet d'aminopeptidases plasmatiques.
La sécrétion de la rénine est réglée
par les variations de la tension intramurale dans l'artériole
afférente et par les modifications dans la composition
ionique de l'urine primitive, perçues au niveau de la macula
densa.
La sécrétion de rénine augmente lorsque la
pression artérielle diminue dans l'artère
rénale - par exemple lorsqu'il y a sténose de l'artère,
hypovolémie ou passage de la position couchée à
la position debout - ou lorsque la concentration de sodium
baisse dans la lumière du tube distal. On peut donc dire
que les cellules de la paroi artérielle sont des barorécepteurs
et que les cellules de la macula densa sont des chémorécepteurs.
L'augmentation de la sécrétion de la rénine
par les cellules du coussinet induit une augmentation de l'angiotensine
II.
L'angiotensine II a des effets multiples qui ensemble concourent
à augmenter la pression artérielle. En contractant
les fibres musculaires lisses des vaisseaux et en stimulant le
système nerveux adrénergique, elle réduit
le volume du lit vasculaire. En provoquant la sécrétion
d'aldostérone par les cellules glomérulaires du
cortex surrénalien, et celle d'ADH par la neurohypophyse,
elle entraîne une rétention de sodium et d'eau et
donc une augmentation du volume plasmatique. Par son effet sur
le centre hypothalamique de la soif, elle contribue également
à l'augmentation de ce volume.
Le rein sécrète également l'érythropoïétine,
mais on ignore de quelles cellules rénales provient cette
sécrétion.
L'érythropoïétine est essentielle pour maintenir
un niveau normal d'érythropoïèse: elle stimule
la maturation des érythroblastes et sa production dépend
des variations de la teneur en oxygène des tissus.
Le rôle des reins dans la régulation de l'érythropoïèse
est démontré parce qu'une anémie est fréquemment
associée à de l'insuffisance rénale chronique
et que certaines tumeurs rénales provoquent de la polyglobulie.
Le thymus est essentiellement composé de lymphocytes
et assure un rôle important dans l'immunité tissulaire.
Nous ne reviendrons pas sur sa structure ou sa fonction; nous
reverrons simplement le rôle des cellules épithéliales.
Les cellules épithéliales thymiques ont trois
fonctions: elles forment le squelette de l'organe, elles assurent
un microenvironnement induisant la maturation des thymocytes,
elles libèrent des substances participant cette maturation.
A ce jour, quatre facteurs thymiques principaux, le facteur
sérique, la thymosine, la thymopoïétine
et le facteur thymique humoral ont été purifiés.
Leur origine exacte et leur rôle précis ne sont pas
encore connus. Il est possible que ces quatre facteurs agissent
sur les thymocytes à proximité des cellules qui
les ont synthétisés, il faudrait alors les considérer
plutôt comme des parahormones. Il est aussi possible qu'ils
agissent à distance sur les lymphocytes du sang et sur
les zones thymodépendantes des organes lymphoïdes
périphériques.
Le nom de prostaglandine a été donné
en 1930, par le physiologiste suédois Von Euler, à
une substance acide, liposoluble, présente dans la vésicule
séminale, le sperme et la prostate. Aujourd'hui, ce terme
recouvre un groupe d'acides gras, présents dans
de très nombreux organes. Le plus souvent, les prostaglandines
sont utilisées par la cellule qui les synthétise
ou par les cellules voisines. Elles peuvent donc être considérées
comme des parahormones. Leur production est difficile à
évaluer et leur concentration sanguine est très
faible.
Les prostaglandines dérivent de l'acide arachidonique.
Elles ont toutes 20 atomes de carbone et un noyau cyclopentane
à deux chaînes latérales. Elles sont classées
en séries A, B, E, et F, en fonction des variations de
leur cycle. On les classe également en sous-séries
en fonction du nombre de doubles liaisons dans les chaînes
latérales et de la position du groupement hydroxyle du
carbone 9.
Voici, à titre d'exemple, la structure de deux prostaglandines
de séries différentes.
L'acide arachidonique est un acide gras poly-insaturé indispensable,
présent dans les phospholipides des membranes cellulaires
et dont il est libéré par une phospholipase. Les
enzymes regroupées sous le nom de prostaglandine-synthétase
ou cyclo-oxygénase, permettent la conversion de l'acide
arachidonique en endoperoxydes. Ces derniers sont des corps instables
à partir desquels se forment soit les prostaglandines proprement
dites, soit d'autres dérivés, les thromboxanes dans
les plaquettes, et les prostacyclines dans les vaisseaux.
Certaines prostaglandines ont un effet local et général
dans les processus inflammatoires. Leur concentration est
accrue dans les zones enflammées où elles provoquent
une vasodilatation et une augmentation de la perméabilité
capillaire. Leur injection induit un accroissement de la température
corporelle, en agissant sur l'hypothalamus. L'action anti-inflammatoire
de certains médicaments comme les glucocorticoïdes
et l'aspirine peut, en partie au moins, s'expliquer par leur action
inhibitrice sur la synthèse des prostaglandines.
D'autres, et notamment les prostaglandines El, E2 et F2 provoquent
la contraction du myomètre et ont été utilisées
pour induire l'accouchement. D'autres, par contre, provoquent
le relâchement des muscles lisses, notament dans les bronches
et les vaisseaux.
Les prostaglandines synthétisées par les reins
augmentent le débit sanguin rénal et le débit
urinaire, en provoquant une vasodilatation. Elles s'opposent donc
à l'angiotensine II qui induit une vasoconstriction rénale.
Les prostaglandines, thromboxanes et prostacyclines participent
ensemble à la régulation de la formation du clou
plaquettaire. Les prostaglandines et les prostacyclines l'inhibent
tandis que les thromboxanes la favorisent et induisent en outre
une vasoconstriction localisée à l'endroit du thrombus.
Enfin, les prostaglandines modulent l'action de nombreuses autres
hormones, mais on ignore encore comment.
 Les cellules C ou claires
ou parafolliculaires sont volumineuses, leur cytoplasme est plus
clair que celui des cellules folliculaires, d'où leur nom.
Leur noyau est pâle et ovoïde. Elles sont enchâssées
dans l'épithélium folliculaire, mais ne viennent
jamais en contact avec le colloïde. Elles peuvent aussi former
des amas dans le chorion.
Les cellules C ou claires
ou parafolliculaires sont volumineuses, leur cytoplasme est plus
clair que celui des cellules folliculaires, d'où leur nom.
Leur noyau est pâle et ovoïde. Elles sont enchâssées
dans l'épithélium folliculaire, mais ne viennent
jamais en contact avec le colloïde. Elles peuvent aussi former
des amas dans le chorion.





