Le système digestif (Cours 8)
 Le foie est le
plus volumineux des viscères. Il est la glande annexe
la plus volumineuse du tube digestif née comme lui de l'endoderme
primitif. Il occupe principalement l'hypochondre droit où
il est recouvert par le diaphragme. C'est un organe asymétrique,
de forme irrégulière. Il est subdivisé en
quatre lobes dont la séparation n'est visible qu'a sa face
inférieure.
Le foie est le
plus volumineux des viscères. Il est la glande annexe
la plus volumineuse du tube digestif née comme lui de l'endoderme
primitif. Il occupe principalement l'hypochondre droit où
il est recouvert par le diaphragme. C'est un organe asymétrique,
de forme irrégulière. Il est subdivisé en
quatre lobes dont la séparation n'est visible qu'a sa face
inférieure.
Le foie sécrète la bile qui, par un système
de canaux excréteurs, est déversée dans le
duodénum. Outre la bile, le foie libère dans la
circulation veineuse une série de produits. Ceuxci
sont le résultat des fonctions métaboliques importantes
remplies par le foie. Ces fonctions sont abondamment décrites
en biochimie. Nous n'en rappellerons que l'essentiel à
la fin du cours. Pendant la vie embryonnaire, le foie est aussi
un organe hématopoïétique, mais il perd
cette fonction dès avant la naissance.
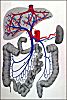 Véritable éponge remplie de sang, le foie
reçoit la veine porte. Celleci est le confluent
de la grande veine mésentérique et de la
veine splénique, ellemême alimentée
par la petite veine mésentérique. La veine porte
se divise dans le foie en un réseau de sinusoïdes
drainé à son tour par les veines sushépatiques
qui se jettent dans la veine cave inférieure sous
la coupole diaphragmatique. Le foie est également alimenté
par l'artère hépatique. Celleci provient
du tronc coeliaque et son réseau capillaire est en continuité
avec les sinusoïdes veineux.
Véritable éponge remplie de sang, le foie
reçoit la veine porte. Celleci est le confluent
de la grande veine mésentérique et de la
veine splénique, ellemême alimentée
par la petite veine mésentérique. La veine porte
se divise dans le foie en un réseau de sinusoïdes
drainé à son tour par les veines sushépatiques
qui se jettent dans la veine cave inférieure sous
la coupole diaphragmatique. Le foie est également alimenté
par l'artère hépatique. Celleci provient
du tronc coeliaque et son réseau capillaire est en continuité
avec les sinusoïdes veineux.
Le foie occupe donc une position stratégique dans la circulation
sanguine. Il est situé sur le parcours sanguin entre le
tube digestif et la veine cave inférieure.
 Examinons une coupe de foie de porc
à faible grossissement. L'organe est entouré d'une
capsule conjonctive fibreuse: la capsule de Glisson dont
les prolongements divisent le foie en petites unités ou
lobules. Chacun de ces lobules polyédriques, larges d'environ
1 à 2 millimètres, représentent une unité
structurelle et fonctionnelle du foie.
Examinons une coupe de foie de porc
à faible grossissement. L'organe est entouré d'une
capsule conjonctive fibreuse: la capsule de Glisson dont
les prolongements divisent le foie en petites unités ou
lobules. Chacun de ces lobules polyédriques, larges d'environ
1 à 2 millimètres, représentent une unité
structurelle et fonctionnelle du foie.
Au centre de chaque lobule,
se trouve une veine plus large, la veine centrolobulaire,
indiquée par une flèche. Elle est habituellement
dépourvue de paroi conjonctive sauf si elle est proche
d'une veine sushépatique. Sa paroi est percée
d'orifices qui mettent sa lumière en communication avec
celle des sinusoïdes drainés par elle et visibles
ici sous forme d'espaces clairs ramifiés. Des lames cellulaires,
très sinueuses et fréquemment anastomosées
entre elles, s'étendent de façon radiaire de la
veine centrolobulaire vers la périphérie du lobule.
Le lobule hépatique,
unité structurelle et fonctionnelle, est constitué
par une série de lames cellulaires à disposition
radiaire et irriguées par un réseau de sinusoïdes
qui confluent dans la veine centrolobulaire. Au carrefour de plusieurs
lobules, la confluence des septa est à l'origine de plages
conjonctives plus importantes. Ce sont les espaces portes de
Kiernan indiqués par les flèches.
Chaque espace porte
contient toujours les trois éléments suivants :
une veinule, une artériole et un canal
excréteur auxquels sont associés quelques vaisseaux
lymphatiques. La veinule est habituellement plus large; sa lumière
est limitée par un endothélium et le reste de sa
paroi se confond avec le tissu conjonctif de l'espace porte. Les
veinules des espaces portes sont toutes des branches de la veine
porte.
La lumière de l'artère est plus étroite et
limitée également par un endothélium. Sa
media est musculeuse. Les artérioles sont toutes des branches
de l'artère hépatique.
L'aspect du canal excréteur varie selon son "calibre".
Sa lumière est limitée par un épithélium
cubique ou cylindrique. En se rassemblant, les petits canaux forment
finalement les canaux hépatiques qui quittent le
foie au niveau du hile.
Dans d'autres espèces que le porc et notamment dans l'espèce humaine,
le tissu conjonctif est réduit aux espaces portes de Kiernan
et aux gaines des veines sus-hépatiques. Les lobules confluent
et leur limite est simplement marquée par une lame cellulaire
un peu plus colorée.
Voyons à présent la structure d'un lobule hépatique.
Les cellules hépatiques, ou hépatocytes,
s'associent entre elles pour former de véritables murs
cellulaires, ou lames, séparés les uns des
autres par des espaces dans lesquels sont logés les sinusoïdes
veineux. Cette image nous montre une vue tridimensionnelle de
ces lames dans deux portions de lobules adjacents.
Les hépatocytes
sont de volumineuses cellules polyédriques. Vingtcinq
pour-cent d'entre elles sont binucléées et
dans les autres, le noyau est souvent tétraploïde.
L'hépatocyte est la cellule de choix pour l'étude
des éléments subcellulaires et son ultrastructure
a été abondamment décrite en cytologie. Nous
n'en rappellerons que l'essentiel.
Voici un fragment d'hépatocyte
observé au microscope électronique. Son noyau
(N) est volumineux et pauvre en hétérochromatine.
Les mitochondries (M) sont nombreuses tout comme les lysosomes
(Ly) au contenu hétérogène. Le réticulum
endoplasmique et le système de Golgi sont bien développés.
L'abondance de ces organites traduit l'importante activité
cellulaire.
Les inclusions lipidiques sont relativement rares dans une cellule
hépatique normale. Par contre, la fréquence des
inclusions de glycogène y est caractéristique.
Le glycogène
se présente comme de petites particules denses aux électrons,
les particules bêta. Elles s'associent généralement
en rosettes ou particules alpha dont le diamètre
est de l'ordre de 150 manomètres.
Dans cette coupe traitée au P.A.S.,
le glycogène apparaît sous forme de petites taches
rougeâtres. Sa distribution dans le lobule hépatique
et même dans la cellule varie suivant l'état physiologique
du foie au moment de son prélèvement.
Les membranes cellulaires latérales
des hépatocytes sont déprimées par une rainure.
Les rainures de deux hépatocytes adjacents se font face
et ménagent entre elles un petit conduit.
Dans une coupe épaisse colorée et examinée
selon les techniques courantes, ce conduit en vue transversale
a l'aspect d'une tache ovale plus foncée. L'ensemble de
ces conduits est à l'origine des voies biliaires.
Dans une micrographie électronique,
on voit les microvillosités des cellules hépatiques
qui découpent la lumière du conduit. La paroi de
ce petit conduit biliaire est donc constituée par les hépatocytes
euxmêmes.
Ces premières voies biliaires
sillonnent toute la lame hépatique et confluent à
la périphérie du lobule. Là, elles acquièrent
une paroi propre et deviennent ainsi de vrais canaux biliaires
appelés passages de Hering ou "cholangioles".
Ils peuvent être observés dans le lobule ou dans
l'espace porte. Leur lumière très étroite
est limitée par des cellules claires, aplaties dont le
rapport nucléocytoplasmique est élevé. Tous
les cholangioles se jettent dans les canaux biliaires des espaces
portes.
Au niveau des faces externes des lames, les hépatocytes
sont en rapport avec les sinusoïdes veineux. En examinant
à plus fort grossissement la zone de contact
entre cellules hépatiques et cellules endothéliales,
on observe entre elles une fente claire très étroite,
l'espace de Disse. La membrane plasmique des hépatocytes
y projette de très nombreuses microvillosités. Cet
espace n'est guère visible en microscopie optique sauf
dans les conditions pathologiques où il est élargi.
Au niveau de l'espace de Disse,
les prolongements cytoplasmiques des cellules endothéliales
présentent de nombreux pores de taille variable.
Les pores mettent en communication la lumière vasculaire
et l'espace de Disse et favorisent donc les échanges
métaboliques. Ils sont cependant trop étroits
pour permettre le passage des cellules sanguines.
L'espace de Disse contient également quelques fibres
conjonctives. Sur une coupe épaisse, ces fibres peuvent être révélées par l'argent.
Elles dessinent un réseau situé entre les hépatocytes
et les cellules endothéliales des sinusoïdes.
L'irrigation sanguine
du lobule hépatique est à la fois veineuse et artérielle.
Le sang veineux provient d'une veinule de l'espace porte,
remplit les sinusoïdes et est drainé par la veine
centrolobulaire vers une des veines sushépatiques.
Le sang artériel provient de l'artériole
de l'espace porte et se mêle au sang veineux dans les sinusoïdes.
Ceux-ci sont limités par un endothélium fenestré
qui permet des échanges de liquide entre la lumière
vasculaire et l'espace de Disse.
Dans une préparation habituelle,
ces fenestrations ne sont pas visibles. On reconnaît cependant
les cellules endothéliales à leur forme aplatie,
leur rapport nucléocytoplasmique élevé
et leur noyau qui fait saillie dans la lumière du vaisseau.
Voici la zone nucléaire d'une cellule endothéliale
examinée au microscope électronique. Le noyau est
riche en hétérochromatine. Le cytoplasme contient
de nombreuses petites vésicules qui démontrent l'importance
de la pinocytose dans ce type cellulaire.
Voici un autre type de cellules localisées dans le sinusoïde.
Ce sont les cellules de Kupffer
(K) ou macrophages hépatiques. Ils proviennent des
monocytes sanguins.
Leur situation dans les sinusoïdes est très variable.
Ici, le macrophage est dans la lumière (S) du vaisseau
contre une cellule endothéliale (E). Parfois il est situé
entre les cellules endothéliales et ses prolongements cytoplasmiques
peuvent s'engager dans les pores. Il peut encore s'insinuer dans
l'espace de Disse (D) et être en contact direct avec les
hépatocytes. Le rapport nucléocytoplasmique
est peu élevé et le cytoplasme renferme des inclusions
marquées de flèches dans cette micrographie. Leur
taille est variable et leur contenu est hétérogène.
Ce sont des vésicules de phagocytose.
Après une injection intrapéritonéale d'encre de Chine,
les cellules de Kupffer se repèrent très
facilement même à faible grossissement. En effet,
l'encre de Chine est une suspension colloïdale de particules
de carbone très rapidement phagocytées par les macrophages.
Les cellules de Kupffer sont toutes ces cellules situées
dans les sinusoïdes et dont le cytoplasme est rempli de grains
noirs qui peuvent masquer le noyau. Les cellules endothéliales
proprement dites en sont pratiquement dépourvues.
Les cellules étoilées,
encore appelées lipocytes ou cellules de Ito,
sont logées dans l'espace de Disse. Comme leur nom l'indique,
elles émettent de longs prolongements dans cet espace et
entre les hépatocytes. Voici une de ces cellules dans une
coupe semifine où elle est indiquée par une
flèche. Elle se trouve entre un macrophage et un hépatocyte.
Elle est aisément identifiable parce que son cytoplasme
contient de volumineuses inclusions lipidiques. Dans les
conditions normales, ces inclusions ne se voient que dans les
cellules de la périphérie lobulaire.
Voici la même cellule vue au microscope électronique.
Elle est située en dehors d'un sinusoïde et entre
deux hépatocytes. Cette cellule émet de longs prolongements
appliqués contre les cellules endothéliales. Son
noyau est rond et pauvre en hétérochromatine. Son
cytoplasme contient plusieurs gouttelettes lipidiques. Elle pourrait
intervenir dans le métabolisme des graisses et de la
vitamine A. Son réticulum endoplasmique rugueux, semblable
à celui d'un fibroblaste, son origine mésenchymateuse
et sa situation souvent proche des fibres réticulées
semble indiquer qu'elle est aussi à l'origine du tissu
conjonctif intralobulaire.
Les trois types de cellules associées aux sinusoïdes
peuvent donc être différencies grâce aux critères
morphologiques suivants :
- Les cellules endothéliales, véritables
cellules de la paroi des sinusoïdes sont perforées.
Leur rapport nucléocytoplasmique est très
élevé et leur cytoplasme renferme des vésicules
de micropinocytose.
- Les cellules de Kupffer ont un rapport nucléocytoplasmique
faible, une forme irrégulière et leur cytoplasme
contient des inclusions de forme et de densité variables.
- Les cellules de Ito renferment de nombreuses gouttelettes
lipidiques. Leur rapport nucléocytoplasmique est
assez élevé.
 La subdivision du foie en lobules hépatiques, telle
que nous venons de la décrire est classique. Mais d'autres
subdivisions ont été proposées, peutêtre
plus adaptées à la physiologie et à la pathologie.
Les unités les plus souvent envisagées sont: le
lobule porte et l'acinus hépatique.
La subdivision du foie en lobules hépatiques, telle
que nous venons de la décrire est classique. Mais d'autres
subdivisions ont été proposées, peutêtre
plus adaptées à la physiologie et à la pathologie.
Les unités les plus souvent envisagées sont: le
lobule porte et l'acinus hépatique.
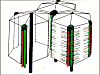
On peut comprendre que la subdivision classique en lobules hépatiques
imaginée par Kiernan et purement anatomique, ne soit pas
suffisante. Si, comme dans ce schéma,
on représente plusieurs lobules dans l'espace, on voit
que chaque lobule est desservi par de nombreuses branches veineuses
et artérielles provenant de plusieurs espaces portes et
que ses conduits biliaires aboutissent à tous les espaces
portes qui l'entourent. Le lobule anatomique est donc, d'un point
de vue physiologique, l'assemblage de plusieurs unités
ou de plusieurs parties d'unités.
Le lobule porte
ou lobule de Sabourin, est le premier essai d'une autre
systématisation. Il est centré sur un espace porte
unique et comprend tout le parenchyme hépatique alimenté
par la veine et l'artère de cet espace. Il est donc un
assemblage de segments appartenant aux différents lobules
hépatiques adjacents à l'espace porte. Les veines
centrolobulaires sont situées en périphérie
du lobule porte.
L'acinus hépatique,
imaginé par Rappaport, est en fait une subdivision du
lobule porte. Il est sans doute l'unité la plus physiologique
du parenchyme hépatique même si ses limites morphologiques
sont très floues. Pour définir l'acinus hépatique,
il faut reprendre la description de l'espace porte. Chaque veinule
et chaque artériole donnent des collatérales qui
sont toutes des branches terminales. L'acinus hépatique
est cette portion du lobule, ou de deux lobules adjacents, qui
dépend de ces branches terminales. La bile de cet acinus
est drainée par un ou deux conduits qui aboutissent au
canalicule biliaire de l'espace porte.
Cet acinus est luimême divisé en trois zones
concentriques. La zone I, la plus proche de l'espace porte,
est celle qui est la mieux vascularisée et où les
échanges entre le sang et les hépatocytes sont les
plus intenses. La zone III est la plus défavorisée
des trois régions car le sang qui lui est destiné
doit d'abord traverser les deux précédentes.
Les principales fonctions du foie sont filtration, activité
métabolique et sécrétion exocrine. Leur
étude détaillée est du ressort de la biochimie.
Le foie filtre une partie du sang artériel de la circulation
générale et la totalité du sang veineux en
provenance de la rate et de l'intestin. L'épuration
est assurée par les cellules de Kupffer, macrophages
particuliers, qui phagocytent bactéries, macromolécules
et corps étrangers amenés par le sang. Comme les
macrophages spléniques, ces cellules participent aussi
au catabolisme des pigments hémiques provenant de la rate.
Grâce à l'activité métabolique intense
des hépatocytes, stockage, transformation, synthèse
et détoxication, le foie joue un rôle de premier
plan dans l'homéostasie du milieu intérieur
.
Il intervient dans le métabolisme énergétique
en accumulant et en libérant des glucides, des protéines
et des lipides.
Véritable usine de transformation chimique, il effectue
certaines réactionsclés et produit des métabolites
intermédiaires qui permettent les conversions entre les
différentes classes de substances biologiques, sur place
et dans les autres tissus.
Le foie est aussi responsable de la synthèse du cholestérol
et de la plupart des protéines plasmatiques.
Enfin, de nombreuses substances d'origine exogène et endogène
subissent une détoxication hépatique. Cette
détoxication fait surtout intervenir des réactions
de conjugaison et d'oxydation qui augmentent l'hydrosolubilité
des substances en cause et facilitent de ce fait leur élimination
par voie rénale ou biliaire. Des réactions d'hydrolyse
inactivent certaines molécules. C'est par synthèse,
grâce au cycle de l'ornithine, que l'ammoniaque s'unit à
l'anhydride carbonique pour former l'urée, déchet
moins toxique du catabolisme protéique.
Le foie est aussi une glande exocrine puisqu'il sécrète
la bile dans le tube digestif. La bile est une solution
aqueuse de pigments biliaires, de sels biliaires, de cholestérol
et de beaucoup de substances provenant des réactions de
détoxication. Les pigments biliaires sont des dérivés
du noyau hémique de l'hémoglobine. Les sels biliaires
proviennent du catabolisme du cholestérol. Outre son rôle
dans l'élimination des déchets du métabolisme,
la bile favorise l'absorption des graisses par l'action émulsifiante
de ses sels biliaires.
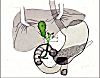 En étudiant l'architecture du foie,
nous avons vu la disposition des voies biliaires intrahépatiques.
Les canalicules biliaires des espaces portes confluent en canaux
de plus en plus grands jusqu'au niveau du hile où il ne
reste que deux canaux biliaires qui s'unissent pour former le
canal hépatique (1). Celuici, est rejoint
par le canal cystique (2) qui draine la vésicule
biliaire (3). Ensemble, ils forment le canal cholédoque
(4) qui se jette dans le duodénum avec le canal de Wirsung.
L'union du canal cholédoque et du canal de Wirsung à
leur entrée dans le duodénum est appelée
l'ampoule de Vater.
En étudiant l'architecture du foie,
nous avons vu la disposition des voies biliaires intrahépatiques.
Les canalicules biliaires des espaces portes confluent en canaux
de plus en plus grands jusqu'au niveau du hile où il ne
reste que deux canaux biliaires qui s'unissent pour former le
canal hépatique (1). Celuici, est rejoint
par le canal cystique (2) qui draine la vésicule
biliaire (3). Ensemble, ils forment le canal cholédoque
(4) qui se jette dans le duodénum avec le canal de Wirsung.
L'union du canal cholédoque et du canal de Wirsung à
leur entrée dans le duodénum est appelée
l'ampoule de Vater.
Les branches du canal hépatique, le canal hépatique
et le canal cholédoque ont fondamentalement la même
structure. Voici la coupe d'un cholédoque.
Sa paroi est composée d'un épithélium
simple formé de hautes cellules cylindriques à
noyau basal entre lesquelles sont insérées des cellules
caliciformes. Cet épithélium repose sur un chorion
lâche, riche en fibres élastiques non colorées
dans cette préparation.
Dans le canal hépatique et dans la partie initiale du cholédoque,
le chorion est infiltré de quelques cellules musculaires
lisses, disposées en petits faisceaux et orientées
dans tous les sens. Dans la partie terminale du cholédoque,
ces cellules musculaires sont très nombreuses et renforcées
par d'autres cellules musculaires lisses à disposition
circulaire.
La vésicule biliaire
et le canal cystique forment la voie biliaire accessoire. Réservoir
piriforme appliqué contre la face inférieure du
foie, la vésicule imprime à sa surface une dépression
large et peu profonde: la fossette cystique. A ce niveau, elle
en est séparée par un tissu conjonctif lâche,
riche en nerfs, en vaisseaux sanguins et vaisseaux lymphatiques.
Sa face libre par contre, est recouverte par le péritoine
qui revêt la face inférieure du foie
On distingue trois parties à la vésicule : une partie
inférieure ou fond (l), une partie moyenne ou corps
(2) et une partie supérieure ou col (3), suivie
du canal cystique.
La paroi de la vésicule
est constituée d'une muqueuse, d'une couche musculaire,
d'une couche périmusculaire et, suivant les endroits, d'une
séreuse.
La muqueuse vésiculaire est sillonnée de
nombreux replis anastomosés dont l'axe, formé par
le chorion, est recouvert par un épithélium cylindrique.
Chez l'homme, l'épithélium s'invagine très
profondément dans la muqueuse pour former des diverticules
souvent confondus avec des glandes. Dans certains cas pathologiques,
ces cryptes s'étendent à la musculeuse et sont appelées
"sinus de RokitanskyAschoff".
Le chorion, bien vascularisé, contient au niveau
du col des glandes muqueuses tubuloacineuses qui s'étendent
en partie dans la couche musculaire. Leur sécrétion
donne à la bile son aspect muqueux. Les glandes ne sont
pas visibles dans cette préparation prélevée
au niveau du corps de la vésicule.
La couche de muscles est fort irrégulière
et ne mérite pas vraiment l'appellation de musculeuse.
Elle est formée d'un réseau de faisceaux musculaires
lisses orientes de façon variable. Les faisceaux musculaires
sont séparés par des fibres élastiques et
collagènes, des fibroblastes, des vaisseaux sanguins et
lymphatiques.
Le tissu conjonctif sousjacent est dense et richement
irrigué. Il entoure complètement la vésicule.
Suivant les endroits, il se confond avec le tissu conjonctif qui
le sépare du foie ou est recouvert d'une séreuse.
L'épithélium de la vésicule biliaire
est formé de hautes cellules cylindriques à
noyau basal. Il est pratiquement dépourvu de cellules caliciformes.
La structure des cellules cylindriques est en relation avec leur
fonction d'absorption. Leur pôle apical est en effet muni
d'un plateau strié. Les microvillosités qui
forment ce plateau sont cependant plus courtes et plus nombreuses
que celles des cellules absorbantes intestinales et ne sont pas
visibles à ce grossissement.
Les parties supérieures des faces latérales de deux
cellules voisines sont unies par des complexes de jonction visibles
dans cette coupe épaisse sous forme de petits points rouges.
Les parties moyennes et basales sont irrégulières
et séparées par un espace intercellulaire. Celuici
nous apparaît en microscopie optique comme une fine fente
claire. L'importance de cet espace dépend de l'état
physiologique de l'épithélium. Tous les processus
d'échange permettant la concentration de la bile ne sont
pas connus, mais on sait que les ions sodium sont pompés
activement vers l'espace intercellulaire. Le gradient de concentration
ainsi créé entraîne simultanément le
passage d'eau de la cellule vers les espaces intercellulaires
qui se dilatent. L'eau et les sels sont ensuite drainés
par les capillaires sanguins appliqués au pole basal des
cellules épithéliales.
La vésicule biliaire est donc un réservoir qui
permet le stockage et la concentration de la bile sécrétée
par le foie de façon continue. Sous l'influence de
la cholécystokinine, elle expulse la bile concentrée.
La cholécystokinine est une hormone produite dans la muqueuse
de l'intestin grêle lors du passage de lipides dans la lumière
intestinale.
 Le foie est le
plus volumineux des viscères. Il est la glande annexe
la plus volumineuse du tube digestif née comme lui de l'endoderme
primitif. Il occupe principalement l'hypochondre droit où
il est recouvert par le diaphragme. C'est un organe asymétrique,
de forme irrégulière. Il est subdivisé en
quatre lobes dont la séparation n'est visible qu'a sa face
inférieure.
Le foie est le
plus volumineux des viscères. Il est la glande annexe
la plus volumineuse du tube digestif née comme lui de l'endoderme
primitif. Il occupe principalement l'hypochondre droit où
il est recouvert par le diaphragme. C'est un organe asymétrique,
de forme irrégulière. Il est subdivisé en
quatre lobes dont la séparation n'est visible qu'a sa face
inférieure.



